Il pH e l’acqua

La qualità dell’acqua ed il valore pH sono sempre di più menzionati insieme. Il pH è un fattore molto importante, perché certi processi chimici possono avvenire soltanto quando l’acqua ha determinato pH. Per esempio, le reazioni del cloro avvengono soltanto quando il pH ha un valore compreso tra 6.5 e 8.
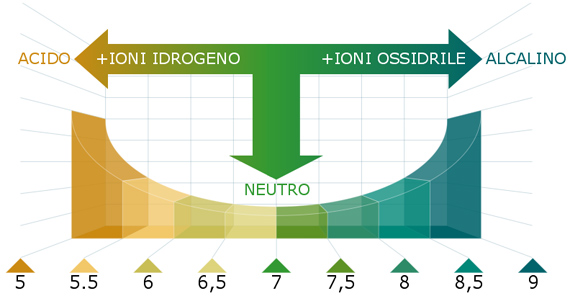
Il pH: esprime il valore di acidità dellacqua. La parola pH è un abbreviazione per "pondus Hydrogenium", che significa letteralmente il peso dell’idrogeno. Il pH è un’indicazione del numero di ioni idrogeno. Quando una soluzione è neutra, il numero di ioni idrogeno è pari al numero di ioni ossidrile. Quando il numero di ioni ossidrile è più alto, la soluzione è basica. Quando il numero di ioni idrogeno è più alto, la soluzione è acida. I Discus vivono in acqua più o meno acida (valore compreso tra ph 4,5 e 6,5), con valori di nitriti, ammoniaca e nitrati praticamente assenti. Nellacquario dei discus spesso si presenta loccasione di dover acidificare lacqua per diversi motivi: per abbassare la carica batterica (è risaputo che il pH basso inibisce lo sviluppo batterico), indurre allo stimolo riproduttivo oppure quando si decide di ospitare esemplari selvatici o addirittura esemplari Heckel (che vivono in acque estremamente acide).
Tendenzialmente, sono sostanze acide tutte quelle in grado di rilasciare ioni H+. Quindi per acidificare l’acqua in acquario si possono usare acidi inorganici come l’acido cloridrico, l’acido fosforico ecc., ed acidi organici come quelli umici, fulvici, ecc. Gli acidi inorganici sono molto più forti ed impongono estrema precauzione nelluso. Gli acidi organici, come la torba, sono più deboli e più facilmente utilizzabili. Personalmente per abbassare il pH faccio uso solamente della torba, infilandone una manciata avvolta in una calza di nylon, direttamente nella prima camera del filtro per una ventina di giorni. Particolare attenzione va fatta sul valore del KH. Per KH elevati o in presenza di ghiaietto che tende a rilasciare carbonati non riusciremo mai ad acidificare lacqua, se non momentaneamente. Infatti col il tempo tutto ritorna come prima. Conviene prima abbassare il KH e sostituire il ghiaietto, con quarzo e poi cominciare ad acidificare. Acidificando con acidi inorganici va tenuto docchio il valore della conduttività che tende a salire. Con acidi organici come gli estratti di torba la conduttivitá non viene modificata. Lacqua RO agli effetti pratici non ha effetti acidificanti, anche se con pH inferiore a 7.
Il KH: indica la durezza carbonatica, o durezza temporanea. In acquariofilia si usa misurarla in gradi tedeschi, °dKH ( 1°dKH corrisponde a 17.8 mg/L o ppm di CaCO3). Il KH misura il contenuto in ioni bicarbonato dell’acquario e quindi la capacità tamponante dell’acquario nei confronti degli acidi e delle basi. Il KH è importante perché il suo valore influenza il valore del pH. Maggiore è la quantità di sali in soluzione, maggiore è il loro potere tamponante; in linea generale un KH superiore a 4 assicura già un sufficiente potere tamponante; resta inteso che valori superiori (diciamo intorno a 6-7) danno una maggior garanzia. Un valore più basso di 4 rende l’acqua dell’acquario instabile e soggetta a pericolose variazioni di pH. E’ forse il caso di far notare che per i cambi d’acqua, mescolare quantità uguali di acqua di rubinetto (ad esempio avente pH 7.5) con acqua ottenuta per osmosi inversa (ad esempio a pH 6.5), produrrà una miscela che avrà un valore medio per quanto riguarda GH e KH, ma che NON avrà un valore medio di pH (cioè NON avrà pH 7.0, tanto per intenderci); la nostra acqua finale avrà ancora un pH di 7.5 perché il potere tamponante degli ioni bicarbonato presenti nell’acqua di rubinetto annullerà del tutto l’acidità dell’acqua osmotica. Il KH si aumenta aggiungendo bicarbonato di sodio. Ricordiamo che la principale fonte di acidità nell’acquario è il ciclo dell’azoto, che è una componente organica dei residui di pesci e piante, viene trasformato in ammoniaca (NH4+, tossica). Successivamente viene trasformata in nitriti (NO2-, meno tossici) e poi in nitrati (NO3-, ancora meno tossici). Il potere tamponante del bicarbonato è tale per cui l’acidità viene rapidamente assorbita ed il prodotto finale resta solo lo ione nitrato, che potrà essere eliminato o attraverso i cambi di acqua, o grazie all’assorbimento da parte delle piante o, molto più raramente, dalla ulteriore riduzione ad azoto gassoso da parte dei batteri anaerobi.
Il GH: indica la durezza dell’acqua, ossia se quest’ultima sia ricca o meno di sali minerali (come calcio e magnesio). Chimicamente misura il contenuto di ioni Ca++ ( calcio ) e Mg++ ( magnesio) dell’acqua. Se l’acqua è ricca di minerali si definisce dura, se povera si definisce dolce. La sua definizione è la stessa data per il KH: 1°dGH corrisponde a 17.8 mg/L di CaCO3 (oppure a 10.0 mg/L di CaO). Si aumenta il GH aggiungendo sali che contengano calcio e magnesio ( ad es. cloruro di calcio, solfato di calcio, solfato di magnesio, ecc) Essendo il GH definito durezza totale, verrebbe da pensare che tra GH e KH sia il primo ad essere sempre prevalente come valore; in realtà questo non è sempre vero. Infatti in alcune acque, come ad esempio quelle dei laghi della Rift Valley in Africa, il KH ha valori superiori, e di molto, al GH; questo è dovuto al fatto che la principale fonte di carbonati, in quei laghi, è il bicarbonato di sodio e non i sali di calcio e magnesio. A seconda dei valori assunti dal GH, le acque possono essere così definite:
| dGH |
ppm |
Definizione |
| 0-4 | 0-70 |
molto tenera |
| 5-8 |
71-140 |
tenera |
| 9-12 |
141-210 |
mediamente dura |
| 13-18 |
211-320 |
abbastanza dura |
| 19-30 |
321-530 |
dura |
| > 30 |
> 530 |
molto dura |
| sistemi di filtraggio comuni | |
| sistemi di filtraggio comuni |



