Il Ciclo dell’azoto 2.0: la teoria

Sul ciclo dell’azoto è stato scritto di tutto, qua è spiegato come si deve:
https://www.mondodiscus.com/2007/09/il-ciclo-dellazoto-2/
Cerchiamo quindi di parlarne in maniera diversa dal solito.
Come succede in tutti gli esseri viventi, le reazioni metaboliche nei batteri sono di sintesi, piccole molecole vengono utilizzate per la sintesi di grosse molecole, che necessitano di energia (anaboliche o endoergonomiche), o di demolizione, grosse molecole vengono demolite in altre di piccole dimensioni, che liberano energia (cataboliche o esoergonomiche).
I batteri si possono dividere in due categorie:
– Batteri eterotrofi che sfruttano il carbonio dei composti organici, fornito da altri organismi viventi, utilizzando l’energia liberata dalla demolizione delle stesse molecole organiche, svolgono ruoli ecologici dipendenti dagli altri viventi come il parassitismo, la simbiosi e il saprofitismo.
– Batteri autotrofi che sono in grado di utilizzare fonti di carbonio inorganico per costruire le proprie strutture cellulari assieme ad un energia di tipo luminoso o derivante dalla demolizione di alcuni composti chimici, in base all’energia sfruttata vengono divise in ulteriori categorie:
1) batteri fotosintetici: effettuano la fotosintesi in presenza di energia luminosa.
2) batteri chemiosintetici: sfruttano l’energia derivante da reazioni chimiche di tipo ossidoriduttivo a livello di alcuni composti presenti nel substrato, sono chiamati anche chemiolitotrofi poiché sfruttano composti inorganici come idrogeno, zolfo, ferro.
Altre divisioni dei batteri, caratterizzate dalla presenza o assenza di ossigeno durante il metabolismo:
– Batteri aerobi che vivono solo in presenza di ossigeno, utilizzato durante la respirazione aerobica come accettatore finale di elettroni.
– Batteri anaerobi facoltativi, per essi non è necessaria la presenza di ossigeno, ma riescono a svilupparsi anche in suo presenza.
–Batteri anaerobi obbligati, vivono solo in assenza di ossigeno, ottengono energia attraverso reazioni cataboliche come la fermentazione e la respirazione.
Il metabolismo catabolico dei batteri avviene tramite fermentazione, respirazione aerobica o anaerobica.
Le fermentazioni sono vie metaboliche alternative alla respirazione; l’acido piruvico, composto organico proveniente dalla demolizione iniziale del glucosio, non è del tutto demolito ed origina dei composti intermedi ricchi di energia, avente come accettatore finale di elettroni un composto organico, essendoci in questa reazione una parziale ossidazione delle molecole organiche iniziali e una parziale liberazione dell’energia in esse contenuta, l’energia disponibile è molto inferiore rispetto a quella della respirazione aerobica.
La respirazione aerobica viene svolta da microrganismi aerobi e anaerobi facoltativi, è un processo attraverso il quale gli esseri viventi, utilizzando l’ossigeno dell’aria, riescono a demolire molecole organiche ricche di energia (zucchero), ossidandole e trasformandole in composti poveri di energia (acqua, anidride carbonica). L’accettatore finale di energia è l’ossigeno, la demolizione dei composti organici comporta la liberazione di un enorme quantità di energia.
La respirazione anaerobica è compiuta da microrganismi che vivono in ambienti dove l’ossigeno scarseggia e che sono in grado di ridurre sostanze come il nitrato e il solfato, queste sostanze diventano gli accettatori di elettroni al posto dell’ossigeno.
Alcuni batteri autotrofi possono compiere il processo fotosintetico e vengono chiamati foto autotrofi, si tratta però di una fotosintesi diversa da quella delle piante superiori e delle alghe, inoltre i batteri usano una clorofilla diversa, detta batterioclorofilla, che assorbe la luce nella regione dell’infrarosso tra i 680 e gli 870 nanometri e si trova in sistemi membranosi accollati alla membrana citoplasmatica. Un’altra differenza è la mancanza della fotolisi dell’acqua e quindi della produzione di ossigeno. La maggior parte di questi batteri infatti è di tipo anaerobico.
Esistono batteri chemioautotrofi in grado di sfruttare l’energia prodotta dall’ossidazione di composti inorganici, senza l’intervento della luce e utilizzando l’anidride carbonica come fonte di carbonio.
Tra i batteri chemiosintetici troviamo i batteri nitrificanti, fondamentali nel ciclo biogeochimico dell’azoto, alcuni ossidano l’ammoniaca a nitriti, altri i nitriti a nitrati, ed i solfo batteri che utilizzano come fonti energetiche composti inorganici dello zolfo come l’idrogeno solforato che viene ossidato a zolfo elementare.
In due parole l’azoto organico biodegradabile è decomposto da batteri eterotrofi ad ammoniaca, alla loro morte la parte organica diviene a sua volta ammoniaca e queste due fonti, sommate all’ammoniaca già presente nell’acqua in entrata nel filtro, sono utilizzate per la crescita di nuovi organismi e convertite dai batteri autotrofi in nitrati.
In acquario dobbiamo avere un sistema di depurazione diverso rispetto alla natura dato che la popolazione ittica è molto superiore, quindi anche la concentrazione degli inquinanti sarà molto maggiore, è necessario avere un efficace sistema di depurazione che trasformi le sostanze tossiche, prodotte dal metabolismo e dai residui di cibo, in sostanze non tossiche.
Da qui la necessità di concentrare dei microrganismi, i vari ceppi di batteri nitrificanti, in un contenitore, il filtro biologico che permette l’ossidazione aerobica di cataboliti azotati, come ammoniaca/ammonio e nitriti, fino a nitrati.
Nel filtro avviene la nitrificazione, cioè l’ossidazione biologica dei composti inorganici dell’azoto grazie ai batteri nitrificanti, che non sono presenti solo nei filtri degli acquariofili, ma anche nei depuratori dei reflui industriali e civili, in ambienta sia dolce che marino e nel suolo.
Batteri Nitrosomas
Batteri Nitrospira
Batteri Nitrobacter
Nel filtro si attua l’ossidazione dei composti inorganici dell’azoto tramite i batteri autotrofi chemiolitotrofi (che trasformano le sostanze inorganiche in materiale cellulare complesso utilizzando la CO2 per la sintesi) e traggono l’energia necessaria al loro metabolismo dall’ossidazione dell’ammoniaca prima e dei nitriti poi, usando l’ossigeno libero come accettare di elettroni, l’ammonio come fonte di azoto e di idrogeno, e bicarbonato di calcio e bicarbonato di potassio come fonte di carbonio, consumano 7.07 grammi di CaCO3 per ogni grammo di NH4+ ossidato.
Sopratutto nelle vasche di nuova installazione succede che sul mangime avanzato si formi della muffa ed il mangime rimane integro per giorni, la formazione di muffa è causata dalla mancanza di fauna eterotrofa che inibisce anche lo sviluppo di altre specie batteriche, per cui aspettiamo invano il picco dell’ammoniaca che non arriva, questo succede perché deve ancora insediarsi la fauna eterotrofa che provvede alla degradazione delle proteine.
La degradazione delle proteine e di altri composti organici azotati sono il risultato del metabolismo di un’ampia varietà di microrganismi, oltre a batteri anche di funghi e attinomiceti.
Gli organismi come alcuni batteri, piante ed alghe che sono in grado di trasformare il carbonio inorganico (come i bicarbonati e la CO2) in composti organici, sono detti autotrofi (che si nutrono da soli), mentre gli organismi che non sono in grado di trasformare il carbonio inorganico in composti organici, sono detti eterotrofi (che non sono in grado di nutrirsi da soli).
I nitrati derivano dalle proteine che di conseguenza sono la principale fonte di inquinamento dell’acquario, i carboidrati ed i lipidi invece vengono degradati in anidride carbonica ed acqua, non contribuendo quindi all’inquinamento del sistema acquario da composti azotati, ma esclusivamente da composti del carbonio come il DOC (Dissolved Organic Carbon).
Gli eterotrofi tramite degli enzimi degradano le proteine in peptidi, poi in amminoacidi ed infine in ammoniaca/ammonio.
Fra i batteri i più attivi sono alcuni clostridi, mentre un minor grado di attività si registra in specie dei generi Proteus e Pseudomonas.
I clostridi si presentano come bastoncini, di solito mobili per mezzo di flagelli; talvolta immobili, formano endospore ovoidali, sono chemioorganotrofi ed alcune specie sono saccarolitiche, alcune proteolitiche, alcune sia saccarolitiche che proteolitiche, sono presenti comunemente nel suolo, nei sedimenti in ambiente di acqua dolce e marina e nel tratto intestinale di uomini e animali.
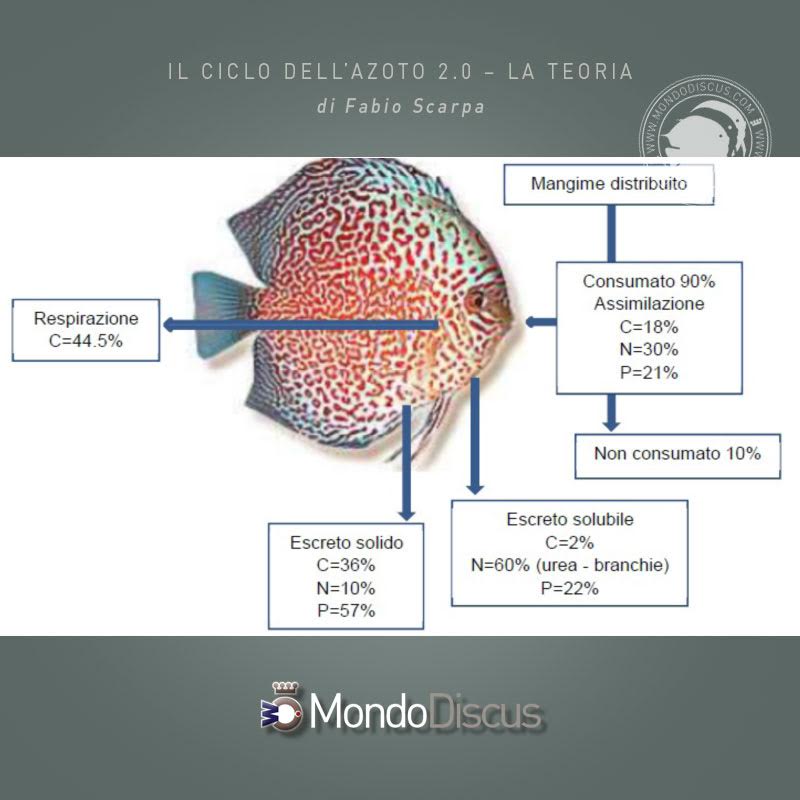
Oltre alle proteine, una sorgente di azoto sono i rifiuti metabolici costituiti principalmente da composti azotati come l’urea, che tramite l’enzima ureasi viene trasformata in ammoniaca/ammonio.
La reazione di ammonificazione è:
H2NCONH2 + 2H2O → 2NH4⁺ + CO3⁻⁻
(urea + acqua → ammonio + carbonato)
Il passaggio seguente è la nitrosazione, consiste nel passaggio da ammonio/ammoniaca a nitrito che si svolge in due fasi, il primo è la monossigenasi che prevede l’ossidazione da ammoniaca/ammonio allo stadio intermedio idrossilammina:
NH4OH + 1/2 O2 → NH2OH + H2O
(ammoniaca + ossigeno → idrossilammina + acqua)
NH4⁺ + 1/2 O2 → NH2OH + H⁺
(ammonio + ossigeno → idrossilammina + ione idrogeno)
La frazione di ammoniaca/ammonio dipende dal pH, in ambiente acido si forma lo ione ammonio che risulta molto meno tossico dell’ammoniaca.
Il secondo passaggio è l’ossidazione dell’idrossilammina a nitrito grazie all’enzima citoplasmatico complesso idrossilamminadeidrogenasi, con il molibdeno come catalizzatore:
NH2OH + O2 → HNO2 + H2O → H⁺ + NO2⁻ + H2O
(idrossilammina + ossigeno → acido nitroso + acqua → ione idrogeno + ione nitrito + acqua).
I principali ceppi batterici responsabili del passaggio appartengono ai generi Nitrosomonas, Nitrosococcus, Nitrosobulos, Nitrosospira.
Questo primo processo esogeno di ossidazione produce quattro volte più energia rispetto al processo di ossidazione del nitrito, 84 kcalmol-1 contro 17.8 kcalmol-1, è irreversibile, consuma ossigeno e produce acidità.
Una volta prodotto lo ione nitrito viene prodotto il substrato necessario per l’attività di un’altra classe di batteri finora inattivi, l’ultimo processo ossidativo del ciclo dell’azoto detto nitrazione è catalizzato dall’enzima nitro ossidasi e comporta l’ossidazione dell’azoto nitroso in azoto nitrico:
NO2– + H2O → NO3– + 2H+
I principali batteri responsabili del passaggio sono i Nitrospira, Nitrobacter, Nitrocystis, Nitrococcus.
Anche questa reazione è possibile solamente in ambienti aerobici ed a differenza della precedente è reversibile in condizioni di anossia.
L’azoto in forma ammoniacale e nitrosa è tossico, oltre che per i pesci, anche per i batteri nitrificanti (Sakairi 1996), la soglia di tossicità dell’ammoniaca non dissociata per i Nitrosomonas è 10 ppm, mentre per i Nitrobacter è di 0.1 ppm, quella dell’azoto nitroso NO2 è di 1 ppm (Saroglia 2001).
Complessivamente le reazioni di ossidazione dell’ammoniaca a nitrati sono:
NH4+ + 2O2 → 2H+ + NO3– + H2O
Considerando che parte dell’azoto è anche richiesto per la sintesi batterica sia dei ceppi Nitrosomas, che dei ceppi Nitrospira, siccome anche il carbonio utilizzato dai ceppi batterici per la sintesi della biomassa, le reazioni stechiometriche su basi teoriche e sperimentali che tengono conto di tutto sono:
- NH4+ + 1.83O2 + 1.98HCO3 → 0.021C5H7O2N + 0.98NO3– + 1.041H2O + 1.88H2CO3
(ammoniaca + ossigeno + bicarbonati → biomassa cellulare + nitrati + acqua + acido carbonico)
- NH4+ + 1.90O2 + 2HCO3 → NO3– + 1.90CO2 + 0.10CH2O
(ammoniaca + ossigeno + bicarbonati → nitrati + anidride carbonica + cellule
e per poter avvenire sono necessari i seguenti equilibri stechiometrici calcolati per l’ossidazione completa di 1 grammo di azoto ammoniacale rispetto la precedente equazione a:
Consumato Prodotto
O2 = 4.18gr H+ = 1.98gr
alcalinità = 7.14gr biomassa cellulare 0.17gr
NO3– = 4.34gr
H2O = 1.34gr
H2CO3 (acido carbonico) = 8.59gr
e secondo la precedente equazione b:
Consumato Prodotto
O2 = 4.33gr H+ = 1.98gr
alcalinità = 7.14gr biomassa cellulare 0.21gr
NO3– = 4.43gr
H2O = 3.73gr
CO2 = 5.97gr
L’ossidazione dell’azoto ammoniacale come si nota determina una riduzione dell’alcalinità carbonatica con produzione di protoni, cellule batteriche, nitrato, acqua ed acido carbonico.
Considerando la prima reazione si consumano 4.18gr di ossigeno per ossidare 1 gr di azoto ammoniacale, si ha una diminuzione di alcalinità corrispondente a 8.63gr di HCO3–, che equivale a 7.07gr di CaCO3, e nello stesso tempo si producono ioni H+ acidi, conseguentemente si ha una tendenza all’abbassamento del pH quando l’alcalinità iniziale dell’acqua, intesa nel nostro caso come KH, non è sufficientemente elevata da tamponare l’acidità prodotta durante la nitrificazione.
Il pH e l’alcalinità carbonatica sono tra i parametri che influenzano maggiormente l’efficienza dei batteri nitrificanti.
Relativamente al primo fattore, il range di tolleranza è compreso tra 6÷9, ma possono resistere a valori di pH sia inferiori che maggiori (5÷10); il campo ottimale è in ambiente neutro/alcalino (7-8) (Kumar e Nicholas, 1983). L’efficienza si riduce proporzionalmente quando il pH scende sotto 7.
Il pH del sistema si abbassa in seguito alla produzione di protoni, e se non viene regolarmente controllato si porterà su valori incompatibili con la buona attività del biofiltro (Summerfelt e Sharrer, 2004).
Il tempo medio di generazione dei batteri nitrificanti è di circa 10/12 ore ed è in relazione con la concentrazione del substrato disponibile nel sistema (Saroglia, 2001) , le attività nitrificanti sono esaltate dalle alte temperature mentre le basse temperature, sebbene non arrestino il processo, ne determinano un rallentamento, il range termico ottimale allo sviluppo dei nitrificanti è tra 25÷35°C, una diminuzione di 6°C dimezza la velocità di crescita massima della biomassa batterica.
A parità di condizioni generali, il rendimento delle specie batteriche presenti nei biofiltri sarà maggiore quindi in condizioni termofile piuttosto che a basse temperature.
E’ stato dimostrato inoltre che in condizioni di portata e carico organico stabile, l’efficienza della nitrificazione è maggiore, è chiaro che “esperimenti” di modifica della portata del filtro e cambi d’acqua frequenti vanno a discapito della nitrificazione e devono essere eseguite nel maniera meno invasiva possibile.
Essendo la nitrificazione un processo aerobico, l’ossigeno disciolto è un fattore limitante per fortuna facilmente controllabile, una buona attività nitrificante è garantita con una concentrazione di 5/6ppm, mentre è inibita a sotto le 2ppm.
Un fattore poco importante è la concentrazione salina, direttamente collegata alla conduttività dell’acqua, concentrazioni fino a 5gr/l non creano problemi all’efficienza batterica.
Per avere un’idea della concentrazione salina, e per possibili conversioni tra le varie scale di durezza:
1° tedesco di durezza (1° d) = 10mg/l CaO
1° inglese di durezza (1° e) = 14.3 mg/l CaCO3
1° francese di durezza (1° f) = 10mg/l CaCO3
fattori di conversione 1° d = 1.25° e = 1.78° f = 0.178mmol/l
Un fattore trascurato invece è l’illuminazione, nei filtri biologici bisogna evitare che la luce, ossidando il citocromo-C batterico, inibisca lo sviluppo dei batteri nitrificanti, principalmente dei nitrosanti, bisogna di conseguenza provvedere ad oscurare il settore del filtro che contiene i supporti biologici.
I supporti biologici vengono definiti a bassa densità quelli che hanno uno sviluppo superficiale da 100÷400 m2/m3, e ad alta densità quelli con uno sviluppo superficiale 400÷2000 m2/m3 (Saroglia 2001).
I sinterizzati sono un gruppo a parte perché lo sviluppo superficiale varia enormemente a seconda delle porosità aperte, per chi volesse approfondire questo argomento ci sono due articoli specifici nel portale.
In letteratura è nota (Ramadori R. e Tandoi V.) anche una nitrificazione eterotrofa, cioè realizzata da microrganismi che necessitano di carbonio organico per la crescita (Arthrobacter, Pseudomonas
aeruginosa, Hansenula mrakii, Aspergillus flavus), che però avviene con una cinetica di due, tre ordini di grandezza inferiore a quella chemolitotrofa, di conseguenza è quasi ininfluente.
leggi la seconda parte:
L’ Influenza del Carbonio

| Pets Festival 2014-Piacenza: il Reportage | Il Ciclo dell’azoto 2.0: l’influenza del Carbonio |
| Pets Festival 2014-Piacenza: il Reportage | |
| Il Ciclo dell’azoto 2.0: l’influenza del Carbonio |

